DIY batteri: fra citron, mønter, kartofler, krukker
Måske vil dette for nogle være en opdagelse lige så betydningsfuld som Columbus opdagelse af Amerika, at der er elektricitet overalt omkring os. Det gennemsyrer bogstaveligt talt hele vores liv. Men selv at vide dette forhindrer nogle gange ikke vores øjne i at brede sig, når vi lærer, at spændinger kan opnås fra de mest almindelige ting og endda fra mad. Ved at bruge det, du har i køkkenet eller garagen, er det ganske muligt at bygge et simpelt batteri derhjemme. 
Artiklens indhold
citron batteri
Selv fra denne frugt kan du få elektricitet. For at gøre dette skal du forberede følgende ting:
- en citron;
- et stykke af noget stål;
- noget lavet af kobber;
- og to stykker ledning til isolering.
Først skal vi rense vores stål- og kobbergenstande. Almindelig sandpapir vil hjælpe med dette.
Reference. En genstand lavet af stål kan være de mest almindelige søm. Der er masser af dem i enhver garage. Og til "noget lavet af kobber" kan du bruge mønter i pålydende værdier på ti og halvtreds kopek.
Nu stikker vi et søm og en mønt ind i citronen. Mellem dem skal du lave et hul på omkring tre centimeter. Disse vil være vores elektroder, det eneste, der er tilbage, er at forbinde ledningerne til dem. Du kan bare sætte den lige ved siden af. Mønten er vores positive kontakt, og sømmet er derfor negativt. 
Reference. Citron kan med held erstattes med et almindeligt æble.Det vigtigste er at vælge den mest sure, som du ikke har noget imod at bruge til eksperimenter. Og syren er nyttig til at reaktionen kan fortsætte.

Et citron- eller æblebatteri (hvis du kun tager én frugt) vil producere omkring 0,5 eller 0,7 volt. Dette er meget lidt - du kan ikke oplade selv den enkleste mobiltelefon. Du skal på en eller anden måde bringe spændingen til tre eller endda fem volt. Men hvordan? Ja, det er meget enkelt - forbind flere frugter i en enkelt kæde.
Reference. For at øge ladningen af vores kredsløb, kan den oplades. Det er nok at inkludere et kronebatteri eller endda en mobiltelefonoplader i kredsløbet.

At få citroner eller æbler til at producere elektricitet bliver muligt, fordi kobberelementet interagerer med stålelementet. Syren indeholdt i frugten udløser denne reaktion. Så længe der er mindst en dråbe syre inde eller så længe kontakterne er intakte, vil batteriet fortsætte med at fungere.
Elektricitet i en bank
Selv fra en almindelig dåse kan du bygge noget, der ligner det allerførste batteri i verden. For at gøre dette skal du bruge:
- en simpel glaskrukke (du kan bruge et glas);
- zink eller aluminium plade;
- strimler af kobber;
- flere ledninger;
- ammoniak, også kendt som ammoniumchlorid;
- postevand.
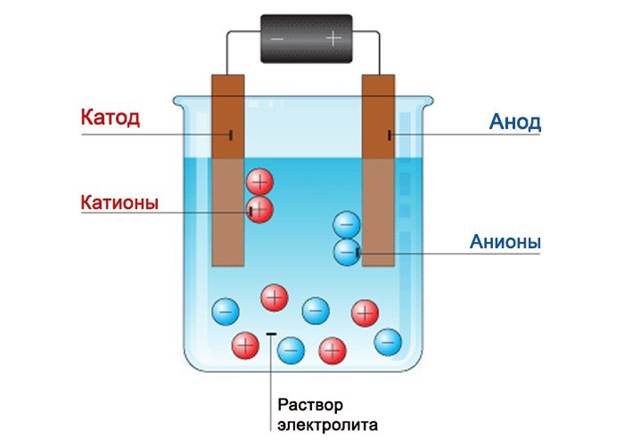
Vores batteri vil have en aluminiumsplade som anode, og en kobberplade vil tjene som katode. Deres størrelse skal vælges, så deres område er lig med håndfladen på en person. Dette vil gøre vores batteri mere effektivt. Lod ledningerne til pladerne. Nu er vores opgave at installere pladerne i krukken, så de ikke rører hinanden. Og højden på disse plader skal være større end selve dåsen.
Det er elektrolyttid. Det er nemt at gøre. Bland ammoniak med vand. For hver 0,1 liter vand skal du tilføje 50 gram pulver.Bland det hele grundigt og hæld i en krukke. I stedet for ammoniak kan du også bruge svovlsyre. For at gøre dette skal det bringes til en tilstand på tyve procent.
Vigtig! Hvis du laver en elektrolyt baseret på svovlsyre, skal du, når du fortynder den, hælde syren i vand, men ikke omvendt. Ellers kan vandet simpelthen koge, og som følge af en voldsom reaktion vil alt sprøjte ud. Derudover skal du ikke glemme, at når du arbejder med syre, skal du bære beskyttelsesudstyr.
Fyld krukken med den resulterende opløsning. Hvis du kombinerer flere dåser i et enkelt kredsløb, får du et meget godt batteri, hvis energi er ganske nok til at oplade en ret kraftig enhed. Dette batteri ligner saltbatterier.
DIY mønt batteri
Selv de mønter, der er i din tegnebog eller sparegris, kan generere elektrisk strøm. Af mønter kan du bygge den enkleste galvaniske celle, som i videnskaben kaldes en voltaisk søjle. Vi skal forberede:
- flere kobbermønter (såsom mønter på halvtreds og ti kopek);
- fødevarefolie;
- flere ark papir;
- bordeddike eller en opløsning af vand og salt.

Lad os nu samle vores energikolonne:
- Vi tager et stykke papir, blødgør det i eddike og fastgør det til en mønt.
- Læg folie på papir.
- Nu igen mønten.
- Indtil vi er færdige med at tilføje mønterne, gentager vi alt sekventielt.
- Som et resultat vil der være en mønt i den ene ende af strukturen. Dette er den positive pol, den anden ende vil have folie. Dette er den negative pol.
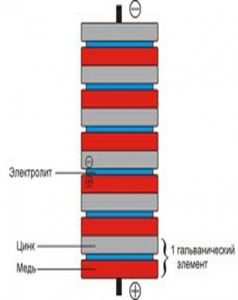
Jo flere mønter du kan samle, jo større er spændingen. Mønterne kan ikke genbruges. Efter eksperimentet vil de allerede være rustne.
Elektricitet i en øldåse
Efter at have drukket dåseøl, skynd dig ikke at smide den tomme dåse. Det vil give et godt batteri. For at gøre dette skal du bruge:
- øldåse (de er lavet af fødevaregodkendt aluminium);
- brændekul eller kulstøv;
- paraffin stearinlys;
- blyant grafit;
- vand og salt;
- et stykke skumplast - skummet skal være mere end en centimeter tykt.
Skær toppen af dåsen af. Vi skærer en cirkel ud af skumplast, så dens diameter passer til krukken. Vi laver et hul i skummet, men ikke igennem. Vi vil installere en grafitstang i hullet. Læg polystyrenskum på bunden af krukken og indsæt stangen. Grafitstangen skal være præcis i midten af dåsen. Vi fylder alt omkring stangen med kulstøv.
Vigtig! Sørg for, at stangen ikke rører krukkens vægge.
Nu laver vi en opløsning af salt og vand. For at gøre dette skal du tage en halv liter vand og tilsætte tre spiseskefulde salt i det. Bland det hele grundigt, så alt saltet er helt opløst. Det opløses hurtigere og bedre, hvis vandet opvarmes. Vi hælder vores elektrolyt i en krukke og forsegler alt med paraffin. Grafitstangen skal stige over dåsens niveau.
Vi forbinder en ledning til stangen - dette er den positive kontakt. Og den anden ledning til dåsens væg er den negative kontakt.Hvis du laver et kredsløb af to dåser, kan du få en spænding på tre volt. Dette batteri kan drive en pære.
Kartoffel batteri
Hvis du har kartofler derhjemme, så er det en ret energisk ting. Sand, engangsbrug. Kartoffelbatteriet kan kun bruges én gang. For eksempel på en vandretur.
For at få batteriet forbereder vi følgende elementer:
- du skal bruge store kartofler;
- kobbertråde i isolering;
- tandpasta;
- træflis eller tandstikker;
- bordsalt.
Skær kartoflerne i to dele. Det er tilrådeligt at gøre dette på langs for at få et større skæreområde. Skær kernen ud i den ene halvdel for at skabe et hul. Placer en blanding af tandpasta og salt i dette hul. Sammensætningen skal fylde hele fordybningen. Denne blanding vil fungere som en elektrolyt.
Vi laver to huller i et andet stykke kartoffel. Afstanden mellem hullerne skal være sådan, at begge er placeret over elektrolytblandingen, når begge halvdele er forbundet. Disse huller er nødvendige til ledninger. Enderne af ledningerne skal strippes for isolering til en længde på to centimeter. Nu forbinder vi begge dele af kartoflerne, og for at de ikke falder fra hinanden, fikserer vi dem med tandstikker.
Vi venter fem minutter på, at reaktionen begynder. Nu lukker vi ledningerne og ser en gnist for enden. Sådan kan du trygt tænde bål med et kartoffelbatteri ved et campingstop.
Konklusion
Naturligvis kan alle de overvejede batterimuligheder, selvom de fungerer, ikke fuldt ud erstatte hverken et batteri eller en akkumulator. Men hvem forhindrer dig i at lave sådanne eksperimenter for bedre at forstå strukturen af disse fysiske elementer og kemiske processer?





